Ny biologisk behandling er ikke kostnadseffektiv
En ny biologisk medisin til behandling av pasienter med psoriasisartritt ble i november 2017 også godkjent for bruk av crohnspasienter. Beslutningsforum for nye metoder mener den ikke er kostnadseffektiv og godkjente den ikke for bruk i spesialisthelsetjenesten.
Statens Legemiddelverk ga mot slutten av 2017 Stelara (ustekinumab) en godkjent metodevurdering i Norge for behandling av Crohns Sykdom. Godkjenningen er gitt for behandling av voksne pasienter med moderat til alvorlig aktiv sykdom.
Medisinene kan brukes i behandling av de pasientene som har hatt utilstrekkelig effekt, har mistet effekten, eller som ikke har tålt konvensjonell behandling eller andre TNF-hemmere (biologisk medisin). Godkjenningen gjelder også de som av andre medisinske grunner ikke kan benytte slike behandlinger.
Tilsvarende effekt
Metodegodkjenningen fra Legemiddelverket og markedsføringstillatelsen for bruk til Crohns- og PsA-pasienter gjelder fortsatt.
– Siden effekten er antatt å være tilsvarende dagens biologiske legemidler, mener Legemiddelverket at Stelara kan inngå i LIS-anbudet på samme vilkår. Det er ikke dokumentert at Stelara er kostnadseffektiv behandling dersom det er dyrere enn andre biologiske legemidler til tilsvarende bruksområde, skriver de i sin metodevurdering fra november 2017.
De mener kriteriet for kostnadseffektivitet er oppfylt, dersom legemiddelkostnadene ved bruk av den biologiske medisinen er lik, eller lavere pris, enn andre pasientadministrerte legemidler i LIS-anbudet.
– Siden effekten antas å være tilsvarende som dagens biologiske legemidler, mener Legemiddelverket at ustekinumab kan inngå i anbudet på samme vilkår som adalimumab (Humira) og vedolizumab (Entyvio). (…) Effekten av ustekinumab sammenlignet med Infliksimab (Remicade/Zessly/Remsima/Inflectra) er ikke dokumentert.
LES OGSÅ: Påvirkning av signalveier kan gi mindre plager for de med Crohns sykdom
For høy pris
Beslutningsforum for nye metoder godkjente den likevel ikke bruk i spesialisthelsetjenesten, fordi det finnes andre biologiske medisiner med tilsvarende effekt, til en lavere kostnad. For Stelara ble det ikke sendt inn tilbud i forbindelse med de offentlige anbudsrundene for biologisk behandling i år. Det får konsekvenser for psoriasisartrittpasientene også.
Stelara vil fremover kun være tilgjengelig til maksimal utsalgspris fra apotek og skal normalt ikke brukes ved nyforskrivning, opplyses det om i de nye LIS-anbefalingene for biologisk medisin for 2018/2019.
Stelara har ifølge Felleskatalogen godkjent metodevurdering for både Crohns- og PsA-pasienter. Det finnes mange ulike biologiske preparater, og LIS-listene nevner bare de som er anbefalt med tanke på lavest mulig pris. Det betyr at det kan finnes flere alternativer som er godkjent for behandling av de ulike diagnosene, men som ikke står i anbudslistene akkurat nå.
Slik fungerer systemet
Systemet Nye Metoder gjelder for bruk i spesialisthelsetjenesten og har to nivåer, et nasjonalt og et lokalt. Alle kan forslå metoder for nasjonal metodevurdering. Folkehelseinstituttet og Legemiddelverket lager metodevarsler, som legges frem for noe som kalles Bestillerforum RHF. Etter klarering der, oversendes de nasjonale metodevurderingene til de regionale helseforetakene, ved fagdirektørene, for beslutning. De har et Beslutningsforum for nye metoder, som avgjør om metoden kan tas i bruk eller ikke i spesialisthelsetjenesten. Der skriver de i sin beslutningsprotokoll fra mai 2018:
– Beslutningen som er fattet er et resultat av en lang prosess og en grundig vurdering av de menneskelige konsekvenser som følger både av beslutning om innføring, så vel som beslutning om å ikke innføre en behandlingsmetode. (…) Usekinumab (Stelara) innføres ikke nå til behandling av Crohns sykdom. Legemiddelet kan imidlertid inngå i fremtidige LIS-anbud.
De skriver også at dersom det tilkommer nye opplysninger (herunder innføring av nye biotilsvarende medikamenter, pasientsikkerhet, kostnadseffektivitet, overlevelsestall mm.) som endrer resultatet vesentlig, vil beslutningen kunne vurderes på nytt.
BLI FAST LESER AV SPONDYLITTEN FOR BARE 100 KRONER UT ÅRET!
– Meget velkommen
– Stelara er den første biologiske behandlingen av Crohns sykdom som retter seg mot interleukin (IL)-12 og IL-23 cytokiner, som man vet spiller en nøkkelrolle for inflammasjon- og immunrespons, skrev legemiddelfirmaet Janssen-Cilag International i en pressemelding i fjor.
– Dagens behandlingsalternativer ved Crohns sykdom er begrenset, og et stort antall pasienter har ikke ønsket effekt og oppnår ikke tilfredsstillende sykdomskontroll med de legemidlene som er tilgjengelig. Et nytt legemiddel med en ny virkemekanisme for å påvirke betennelsen i tarmen er derfor meget velkommen, uttalte Jørgen Jahnsen i pressemeldingen.
Han er overlege ved avdeling for fordøyelsessykdommer, Akershus universitetssykehus og professor i gastroenterologi, Universitetet i Oslo.
LES OGSÅ: Bekhterevs sykdom og mageproblemer
Pasientadministrert
Legemiddelverkets metodegodkjenning av medisinen baseres på data fra tre avgjørende Fase III-studier, hvor omlag 1400 pasienter med moderat til alvorlig aktiv Crohns sykdom deltok. Fase 3-studiene viser at en signifikant større andel av pasientene som ble behandlet med Stelara oppnådde klinisk respons allerede etter seks uker. De opprettholdt klinisk bedring etter et års behandling, sammenlignet med kontrollgruppen som fikk placebo.
Bortsett fra den første infusjonen på sykehuset, settes Stelara (ustekinumab) som en subkutan injeksjon av pasientene selv. Startdosen er basert på pasientens vekt og er på minimum dobbel dose, ifølge felleskatalogen.no.
Den første dose pasienten setter selv er på 90 mg, og settes etter åtte uker. Etter dette anbefales det en injeksjon hver tolvte uke. Dersom effekten blir dårlig etter tolv uker, kan det være gunstig å øke frekvensen til hver åttende uke, står det i felleskatalogen.
Sikkerhet og effekt hos barn og ungdom under 18 år er ikke fastslått.
LES OGSÅ: Ikke bare vondt i ryggen!
Bivirkninger
I Norsk legemiddelhåndbok beskrives Stalara (ustekinumab) som et «monoklonalt antistoff som binder seg til subenheten p40 som er felles for de inflammatoriske cytokinene IL-12 og IL-23.» Halveringstiden på en subkutan injeksjon, altså tiden det tar fra medisinen settes til den begynner å miste sin virkning, er på cirka tre uker.
Som alle biologiske medisiner kan også denne føre til bivirkninger. Det betyr ikke at alle får dem. Ved slik immundempende behandling kan det være en økt risiko for infeksjoner. De mest vanlige bivirkningene ved biologisk behandling er å få forkjølelse, hodepine og infeksjoner i øvre luftveier. De fleste av disse er milde eller moderate øvre luftveisinfeksjoner. Andre bivirkninger kan blant annet være diaré, urticaria, munnherpes, rennende nese, munnsopp, fotsopp, ørebetennelse og øyebetennelse.
Det anbefales at man unngår levendebaserte vaksiner. Influensavaksine og pneumokokkvaksine er ikke-levendebasert og kan benyttes.
LES OGSÅ: Aktiv tarmsykdom forbindes med lavt vitamin D
Forsiktighetsregler
Ved bruk av Stelara (ustekinumab) er det også rapportert om vanlige bivirkninger som ryggsmerter, muskelverk, leddsmerter, svimmelhet og tretthet (fatigue), samt rødhet og smerter på injeksjonsstedet. Mindre vanlige er hudavskalling, kviser, utslett, cellulitt, infeksjoner i forbindelse med tennene, utmattelse og depresjon.
- Forsiktighet bør utvises når bruk vurderes hos pasienter med kronisk infeksjon eller historie med gjentatte infeksjoner, eller hos pasienter som har hatt kreftsykdom. Utvikling av kreft har blitt sett i studier av Stelara (ustekinumab).
- Alvorlige overfølsomhetsreaksjoner er rapportert, i enkelte tilfeller flere dager etter behandling.
- Anti-TNF-behandling må vurderes med forsiktighet hos pasienter med hjertesvikt.
STØTT SPAFO NORGES FRIVILLIGE ARBEID
CROHNS SYKDOM
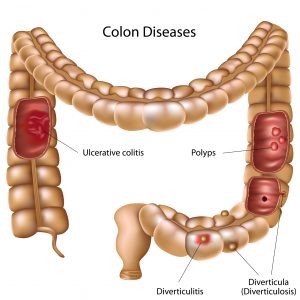
- Crohns sykdom er en kronisk inflammatorisk tarmsykdom som kan oppstå hvor som helst i tarmsystemet. I Norge antar man at cirka 7 000 lever med Crohns sykdom, og at cirka 300 nye personer rammes av sykdommen hvert år.
- Selv om personer i alle aldre kan rammes av Crohns sykdom, er det som oftest i alderen 15 til 35 at sykdommen gjør seg gjeldende. Sykdommen er like vanlig hos menn som hos kvinner.
- Årsaken til Crohns sykdom er ukjent, men sykdommen forbindes med avvik i immunsystemet, som kan utløses av en genetisk disposisjon, eller diett og andre miljøfaktorer. Symptomene på Crohns sykdom er varierende, men vanlige tegn er gjentakende diaré, magesmerter og kramper, ekstrem trøtthet, vekttap, blod og slim i avføringen, samt forstoppelse, sår og analfistler.
Kilde: Janssen-Cilag International
SPESIELLE FORHOLD
- LIS- anbefalingene gjelder ved oppstart av biologisk behandling og ved skifte av legemiddel. Spesielle forhold kan påvirke legemiddelvalg hos den enkelte pasient. Det kan blant annet være forhold som brukervennlighet, spesielle sykdomsmanifestasjoner, reisekostnader, bivirkningsprofil og ønske om graviditet. I slike tilfeller skal behandlende lege begrunne avvik fra føringen om å velge rimeligste alternativ. Denne begrunnelsen skal dokumenteres i pasientens journal.
- Hvis behandlingsmål ikke nås hos den enkelte pasient etter en viss observasjonstid (vanligvis 6 måneder), anbefales endring av behandling. Skifte av legemiddel kan gi reduserte kostnader på grunn av lavere tilbudspris for flere av de aktuelle legemidlene, skriver spesialistgruppen i sine anbefalinger.
- Når doseøkning vurderes på grunn av utilstrekkelig effekt, eller behandlende lege velger en dose som er høyere enn anbefalt dose i preparatomtalen, skal de økte kostnader veies mot forventet helsegevinst ved doseøkning mot skifte av preparat. Ved likt virkestoff anbefales det å gjennomføre bruk av rimeligste alternativ.
Kilde: Spesialistgruppen hos Beslutningsforum for nye metoder